Les tests de stabilité sont une exigence fondamentale dans le développement pharmaceutique, garantissant que les substances médicamenteuses et les produits finis maintiennent leur sécurité, leur efficacité et leur qualité tout au long de leur durée de conservation prévue. AChambre de stabilitéFournit un environnement contrôlé-défini par des conditions précises de température, d'humidité et de lumière (facultatif)-pour simuler des scénarios de stockage à long terme, intermédiaire et accéléré. Pour les fabricants de produits pharmaceutiques, ces chambres ne sont pas simplement des équipements de test, mais des outils essentiels pour la conformité réglementaire, l'atténuation des risques et l'assurance du cycle de vie des produits.
Cet article fournit une ventilation complète des fonctions de la chambre de stabilité, des spécifications techniques, des normes réglementaires, des exigences de validation, et pourquoi les systèmes de haute précision-tels que ceux conçus par l'industrie LIB-jouent un rôle essentiel dans la gestion de la qualité pharmaceutique.
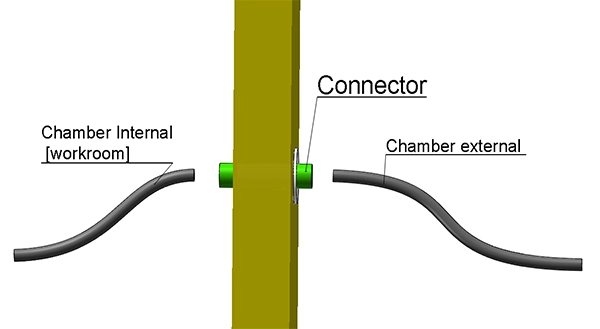
Une chambre de stabilité est un système environnemental contrôlé conçu pour maintenir des conditions de température et d'humidité constantes conformément aux normes internationales de test de stabilité pharmaceutique.
 |  |
Les paramètres de performance typiques incluent:
Plage de température: -20 °C à + 150 °C (plage de température personnalisable)
Précision de la température: ± 0.1 °C
Uniformité de la température: ± 0.5 °C
Gamme d'humidité: 20% RH-98 % HR
Uniformité d'humidité: ± 2.5% HR
Les systèmes peuvent être disponibles comme:
Chambres de stabilité Reach-in (100-1000 L)
Chambres de stabilité sans rendez-vous (5 m³-100 m³)
Chambres de stabilité personnalisées pour emballage pharmaceutique spécial ou charges surdimensionnées
Ces paramètres environnementaux précis garantissent des conditions de test reproductibles et validées pour les formes de dose solide, les injectables, les vaccins, les produits biologiques et les API.
Les produits pharmaceutiques sont confrontés à des risques de dégradation tels que l'oxydation, l'hydrolyse, la photolyse, la transition polymorphe et l'instabilité physique. AChambre d'humidité de la température de stabilitéAide à identifier:
Durée de conservation et dates d'expiration
Exigences de stockage (25 ° C vs 30 ° C par rapport aux conditions réfrigérées)
Aptitude à l'emballage (blister, bouteilles en PEHD, flacons, tubes en aluminium)
Voies de dégradation sous stress Impacts de l'humidité, du cycle de la température et de l'exposition à long terme
Les points de douleur typiques de l'industrie comprennent:
OOS inattendu (hors spécification) causé par une mauvaise uniformité de la chambre
Les tests à long terme de 12 à 36 mois nécessitent une fiabilité élevée
Échec de l'audit en raison des journaux de données incomplets de 21 CFR Part 11
Besoin d'une performance stable dans 24/7 fonctionnement
Test multi-conditions nécessitant plusieurs chambres ou grandes pièces sans rendez-vous
Un système performant minimise ces risques, assurant la précision des données et la conformité réglementaire.
Une chambre de stabilité de qualité pharmaceutique intègre plusieurs caractéristiques mécaniques et de contrôle avancées:
Contrôleur microprocesseur PID Algorithmes d'auto-optimisation Capteurs RTD doubles pour la précision Relais SSR/état solide pour un contrôle de puissance stable |  |
Réfrigérants écologiques Réfrigération à plusieurs étages pour un contrôle serré Contournement de gaz chaud pour une modulation lisse Compresseurs de défilement à faible vibration |  |
Flux d'air laminaire uniforme Ventilateurs à haut rendement fonctionnant à régime constant Vitesse de l'air 1 ~ 2 m/s pour la distribution uniforme | 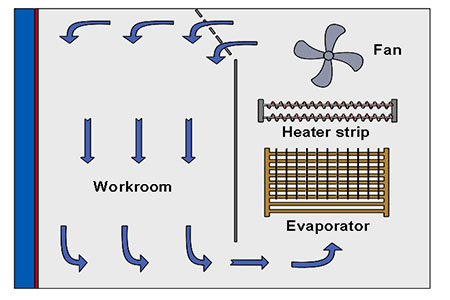 |
304 intérieur en acier inoxydable Isolation en mousse de polyuréthane (épaisseur de 100mm) Joints de porte magnétiques Fenêtres de visualisation facultatives et éclairage LED |  |
Protection contre la température excessive Protection contre l'humidité de l'eau faible Récupération de la mémoire hors tension Alarmes portes ouvertes |  |
Graphiques des tendances en temps réel Exportation de données USB/Ethernet Surveillance à distance |  |
Ces composants mécaniques et numériques assurent une stabilité et une reproductibilité à long terme, en particulier dans les programmes de tests pharmaceutiques de plusieurs mois.
Une chambre de stabilité conforme doit répondre à plusieurs directives internationales. Les principales normes comprennent:
Définit les conditions de test à long terme, intermédiaires et accélérées.
Directives supplémentaires pour les programmes mondiaux de stabilité pharmaceutique.
Utilisé pour les vaccins, les protéines et les produits biologiques.
Enregistrements électroniques et signatures pour l'enregistrement des données.
Exigences européennes et classifications des zones climatiques.
Compétence des laboratoires d'essais et d'étalonnage pour des résultats reproductibles.
Zones climatiques (ICH et OMS):
| Zone | Condition | Application |
| Zone I | 21 °C / 45% HR | Tempéré |
| Zone II | 25 °C / 60% HR | Subtropical |
| Zone III | 30 °C / 65% HR | Chaud/sec |
| Zone IVA | 30 °C / 75% HR | Chaud/humide |
| Zone IVb | 30 °C / 70% HR | Très humide (ASEAN) |
25 °C ± 2 °C / 60% HR ± 5% HR
Durée: 12-36 mois
30 °C ± 2 °C / 65% HR ± 5% HR
Durée: 6-12 mois
40 °C ± 2 °C / 75% HR ± 5% HR
Durée: 6 mois
Une chambre de stabilité doit maintenir ces conditions avec un écart extrêmement faible, garantissant des données précises et prêtes à être vérifiées.
Les chambres de stabilité pharmaceutiques doivent être validées avant utilisation:
Vérification de l'utilité
Nivellement et contrôle structurel
Installation du contrôleur
Vérification des composants
Certificats d'étalonnage
Tests de précision de la température
Tests de précision d'humidité
Validation du système d'alarme et de sécurité
Vérification de la journalisation des données
Tests à pleine charge et à vide
Cartographie avec 9-15 capteurs
Test de stabilité de 72 heures
Vérification de l'uniformité (± 0.5 °C et ± 2.5% HR typique)
La validation garantit un fonctionnement reproductible, fiable et conforme.
Les chambres de stabilité sont utilisées pour:
Comprimés et capsulesInjectables (flacons, ampoules)
Vaccins et produits biologiques
Gouttes oculaires et sprays nasaux
Essais de matériaux d'emballage
Études de matières premières API
Programmes de prolongation de la durée de vie
Analyse de compatibilité des emballages
Chaque catégorie de produit nécessite une tolérance stricte et une fiabilité opérationnelle à long terme.
Les conditions courantes comprennent 25 ° C/60% HR (à long terme), 30 ° C/65% HR (intermédiaire) et 40 ° C/75% HR (accéléré).
La capacité, la plage de température, la plage d'humidité, l'éclairage, les étagères et la conception de porte peuvent tous être personnalisés.
Oui-L'industrie de LIB construit des chambres d'accès et des salles de stabilité sans rendez-vous de 5 m³ à 100 m³.
En général, tous les 6 à 12 mois, selon les SOP du site et les exigences réglementaires.
L'industrie LIB se spécialise dans les équipements de simulation environnementale de précision conçus pour la conformité pharmaceutique.
Les principaux avantages comprennent:
Haute précision: ± 0.1 °C température/± 1.5% HR
HumidityConception de flux d'air optimisée par uniformité
Chambres de stabilité de plain-pied personnalisées jusqu'à 100 m³
Fonctionnement fiable 24/7 à long terme
Documentation complète: IQ/OQ/PQ + étalonnage + schémas de câblage
Installation globale et support à distance (garantie prolongée de 3 ans et service à vie)
Conçues pour un fonctionnement robuste et continu, les chambres de l'industrie LIB aident les sociétés pharmaceutiques à passer des audits, à réduire les événements OOS et à garantir la cohérence de la qualité des produits.
Pour les équipes pharmaceutiques à la recherche de solutions de stabilité de haute précision compatibles ICH, prêtes pour 21 CFR Part 11, l'industrie LIB propose des chambres personnalisées conçues pour une fiabilité à long terme et une conformité réglementaire mondiale. Contactez-nousInquiry@libtestchamber.comPour les spécifications, les options de personnalisation ou une citation formelle.
 English
English русский
русский français
français العربية
العربية Deutsch
Deutsch Español
Español 한국어
한국어 italiano
italiano tiếng việt
tiếng việt ไทย
ไทย Indonesia
Indonesia